经过多年的延迟FDA批准了Teva的通用EpiPen
心脏病发作会使心脏部分永久性地留下疤痕,导致长期的残疾和潜在的心力衰竭。科学家们研究了各种修复或再生受损心脏组织的方法,但收效甚微。
斯克里普斯研究化学家Matthew Disney博士的一项新研究表明,通过靶向一个在衰竭心肌中激增的重要生物分子,有朝一日有可能用药物治愈受损的心脏组织。
在周一发表在《Nature Chemistry》杂志上的一项研究中,Disney团队描述了在细胞模型中发现的第一种能够重启细胞产生VEGF-a(血管内皮生长因子a)因子的化合物。
多年来的研究表明,VEGF-A可以作为干细胞的信号,使它们在受损的心脏组织中重建血管和肌肉,并改善血流。
靶向核糖核酸,即基因和蛋白质生产之间的“中间人”是合乎逻辑的,但用药物这样做曾经被认为是不太可行的。因为 RNAs简单的四碱基结构和动态形状一直被认为是不良的小分子药物靶点。多年来,Disney和同事们开发了一系列的计算和化学工具来克服这些障碍。
“在心脏病发作期间,损伤会导致促进新的健康血管生长的蛋白质变得沉默,”Disney解释道。“我们分析了蛋白质如何被沉默的整个途径,然后我们利用这些信息来确定如何重新激活它的表达。”
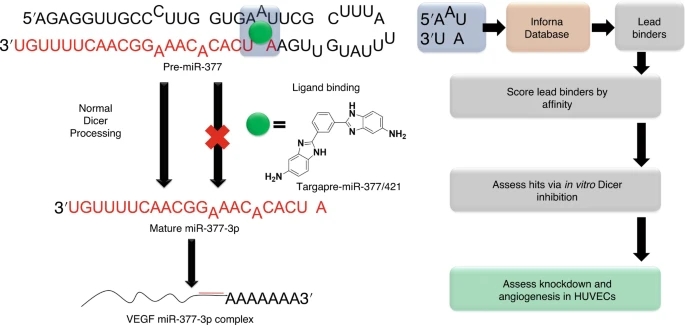
主要作者Hafeez Haniff分析了VEGF-a产生的基因组学,以评估最佳的RNA药物靶点。研究小组选择了一种名为pre-miR-377的microRNA前体,发现其作用类似于衰竭心肌中VEGF-a产生的微调开关。
然后,他们利用Disney的计算和化学工具,结合阿斯利康公司收集的一系列不同的化合物,寻找能够选择性地结合pre-miR-377关键保守结构特征的化学伙伴。
“一个显著的靶向特异性是通过结合活性化合物和其他辅助分子来实现的,”Haniff解释道。
其他促进VEGF-A产生的策略包括给予VEGF-A本身,或传递编码该蛋白的信使RNA。
Disney说:“与潜在的特异性、RNA结合的小分子药物相比,这些方法中的每一种都使用了能够在病变组织中有限分布的大化合物。”
Disney指出,到目前为止,这种化合物已经在细胞中进行了测试,但还没在心力衰竭的整个动物模型中测试。
Disney说,将TGp-377转化为一种有潜力的药物,并使之惠及患者,将需要相当多的时间和研究。”
Disney称他们的成功是一个“试验案例”,表明有可能可靠和可预测地开发出用于预定RNA靶点的药物化合物,并在细胞模型中诱导蛋白质的产生。阿斯利康药物化学、研究和早期开发、心血管、肾脏和新陈代谢部门的负责人MalinLemurell称这是潜在的重要的第一步。他说:“设计能够与RNA相互作用并调节RNA的小分子的能力可能会为靶向具有挑战性的疾病途径开辟新的途径,这些途径以前被认为是不可克服的。阿斯利康生物制药研发部这项研究已经促成了高质量工具化合物的产生,这将有助于进一步探索这种作用模式。”
Disney说:“几乎每种疾病都有潜在的RNA药物靶点。”我们现在有了一个更强大的工具箱来寻找具有药用潜力的铅分子。”
原文检索:Design of a small molecule that stimulates vascular endothelial growth factor A enabled by screening RNA fold–small molecule interactions
(生物通:伍松)
-
合成微生物使科学家们能够研究古老的进化神秘
2022-04-29 -
加强了恰帕斯高地土着居民的领土管理合作进程
2022-04-29 -
介绍CNVP,IUCN的新成员
2022-04-29 -
销售人员为肥胖客户推荐更多圆形产品
2022-04-29 -
黄石麋鹿的疾病隐藏成本 USU生态学家说 布鲁氏菌病会减少怀孕
2022-04-29 -
研究人员设计“智能”表面以排斥一切 但针对有益的例外
2022-04-29 -
大麻使用的性别差异开始在动物和人类的大脑研究的帮助下得到解释
2022-04-29 -
缅甸开始在全国红色名单上工作
2022-04-29 -
转染市场五年后将达到10亿美元
2015-07-08