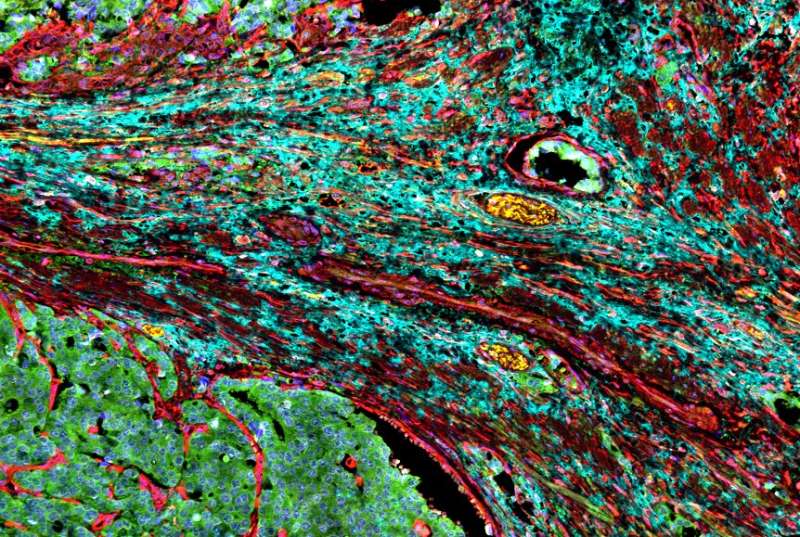
肿瘤释放乳酸,迫使附近的细胞发挥支持作用
Terasaki生物医学创新研究所(TIBI)的研究人员已经转向蚕丝蛋白,蚕丝蛋白(SF),由家蚕生产作为肌腱修复的生物材料。研究人员报告说,他们的方法已经在间充质干细胞(MSCs)肌腱再生方面取得了重大进展。
他们的发现发表在《Small》杂志上的一篇论文中。
SF是一种很有前途的肌腱修复生物材料,但其相对刚性的力学性能和较低的细胞亲和性限制了它在再生医学中的应用。”“同时,明胶基聚合物在细胞附着和组织重塑方面具有优势,但在再生肌腱等硬组织方面机械强度不足。考虑到这些方面,在本研究中,明胶甲基丙烯酰(GelMA)与SF结合,形成机械强度高、生物活性强的纳米纤维支架(SG)。”
肌腱损伤可能的治疗方法包括从患者或捐赠者那里移植肌腱组织,但这些会带来感染、移植排斥或坏死等风险。人工移植已经尝试过,但是机械、生物相容性和生物降解问题阻碍了这些努力。
另一种方法是使用MSCs。然而,使用系统输注、直接注射或基因修饰MSCs的治疗方法可能导致对损伤部位特异性不靶向、细胞数量过高或细胞无法分离。
由于丝素的强度、耐久性、生物相容性和生物降解性,研究小组首先转向了丝素。
为了提高支架的组织再生能力,该团队随后将丝素蛋白与GelMA配对,GelMA是一种基于明胶的保水凝胶,因为GelMA具有生物相容性、可降解性、刚度以及促进细胞附着和生长的能力。
“GelMA支持再生组织形成的能力和丝素蛋白的结构优势的协同作用,使我们的复合材料非常适合肌腱修复,”HanJun Kim博士说,DVM博士,TIBI项目的团队负责人。
他们制备了不同比例的丝素蛋白和GelMA (SG)的混合物,并将它们制成薄的纳米纤维片。然后,他们测试了薄片的纤维结构和弹性,并选择了具有最佳机械性能的最佳配方。他们还观察到丝素使材料的孔隙度增加;这有助于肌腱修复。
与未使用GelMA (SF)的丝素片相比,SG片上的MSCs的细胞活力和增殖能力均有所提高。遗传分析显示,SG MSCs的相关基因活性显著升高,而SF片的相关基因活性则降低。
对植入纳米纤维薄片的间充质干细胞分泌的生长因子的进一步测试表明,SG薄片上的间充质干细胞产生的生长因子能够最好地修复培养皿中培养的损伤肌腱组织。
实验也在跟腱受伤的活老鼠身上进行。
TIBI的主管兼首席执行官Ali Khademhosseini博士说:“肌腱修复的组织重塑尤其难以实现。“这里所做的工作大大推进了这一成就。”
原文标题:
Co-Electrospun Silk Fibroin and Gelatin Methacryloyl Sheet Seeded with Mesenchymal Stem Cells for Tendon Regeneration
-
新方法:在常规临床基因组测序分析中轻松识别肿瘤中的病毒
2022-07-26 -
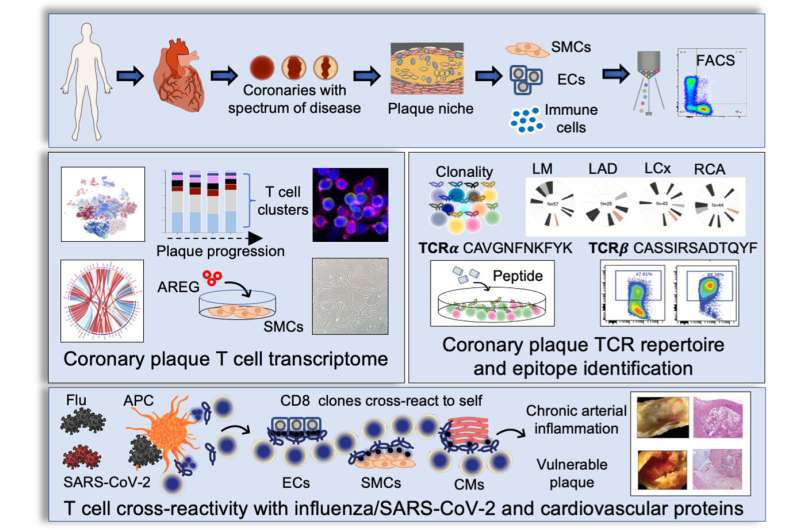
颈动脉斑块内的个体免疫细胞特征
2022-07-26 -
免疫系统癌症研究综述
2022-07-26 -
Nature子刊:根据大量神经成像数据预测大脑年龄
2022-07-26 -
将时间从几个月缩短到几周:一种新的基因传递方法
2022-07-26 -
《Science》四篇论文:绘制人类33个器官中的百万细胞
2022-07-26 -
Nature子刊:线粒体呼吸链维持炎症
2022-07-26 -
Nature子刊:基于电子病历预测心理健康危机的机器学习模型
2022-07-26 -
解决30年难题:科学家发现新的蛋白质结构,帮助合理设计药物
2022-07-26 -
Cell:发现首个在客户金属蛋白上装载锌的伴侣家族
2022-07-26