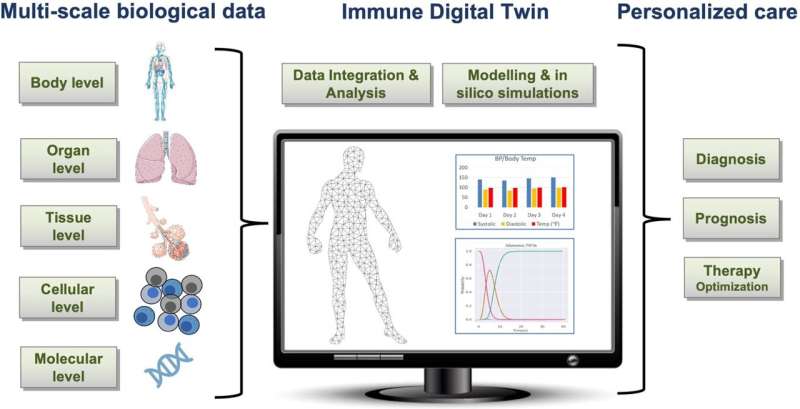
肿瘤释放乳酸,迫使附近的细胞发挥支持作用
在对移植了人类尤因肉瘤组织的小鼠进行的研究中,乔治敦大学医学中心的研究人员及其同事发现了一种生物途径,这种途径在组织因肿瘤的快速生长而缺氧时被激活。因此,癌细胞可以进行基因改变,从而转移到骨骼,即使在接受化疗时也能茁壮成长。
科学家们发现的这一途径涉及癌细胞表面的一种名为Y5R的受体,它在介导缺氧效应中发挥作用——如果它被阻断或关闭,基因变化将受到限制,从而抑制肿瘤的转移。
这一发现于2022年4月28日发表在《自然通讯》杂志上。
在美国,每年大约有200名儿童和年轻人被诊断出患有尤文氏瘤。大约一半被诊断为尤文氏肉瘤的患者年龄在10到20岁之间;几乎所有尤文氏肉瘤都发生在白人和西班牙裔人群中。如果在诊断时肿瘤已经扩散到远处,5年生存率为38%,但如果扩散到骨骼,生存率将下降到8%至14%。
“虽然快速的基因变化在促进癌症增长中的作用是众所周知的,但引发这些变化的机制尚不清楚,也缺乏预防它们的策略。”Joanna Kitlinska博士说,她是乔治敦大学生物化学和分子与细胞生物系的副教授,也是该研究的通讯作者。“这就是为什么我们确定Y5R参与启动这种基因改变是重要的,因为它给我们提供了一个靶向或阻断的目标,可以避免癌症基因组进化,并导致对化疗有耐药性的转移性肿瘤的进展。”
目前尤文氏肉瘤的治疗标准包括系统性细胞杀伤化疗,这种化疗可以影响体内所有细胞,从而导致副作用。在尤文氏肉瘤的常规治疗中,没有针对基因改变的治疗方法,这可能会降低治疗的毒性。特别是,对转移性疾病患者缺乏适当的治疗。
目前有很多针对Y5R的药物,因为Y5R也与调节食物摄入和精神疾病有关。几种Y5R靶向药物已成功用于动物研究;其中一种被用于肥胖症的人体临床试验。然而,它们中的大多数被设计用来阻止大脑中抑制食物摄入的功能。Kitlinska表示,主要的挑战将是设计出不通过血脑屏障的Y5R靶向药物,因为这些效应在癌症患者中是不受欢迎的。
Kitlinska说:“我们将继续在小鼠身上进行实验,以试图确定触发尤因肉瘤扩散到骨骼的机制。尤文氏肉瘤的发现也可能与已知的Y5R高表达的其他癌症类型有关,包括另一种儿童癌症,神经母细胞瘤,以及常见的成年恶性肿瘤,如乳腺癌、前列腺癌和肝癌。”
Hypoxia-activated neuropeptide Y/Y5 receptor/RhoA pathway triggers chromosomal instability and bone metastasis in Ewing sarcoma
-
重编程技术让受损的肝组织更快修复
2022-07-26 -
运动如何对抗糖尿病损害的新证据
2022-07-26 -
细胞重编程改善小鼠肝脏再生
2022-07-26 -
再见了,活检——手持设备可以毫无痛苦地识别皮肤癌
2022-07-26 -
国际研究发现,近13%的COVID-19住院患者有严重的神经症状
2022-07-26 -
作为潜在的神经治疗手段,光遗传学作用可能被夸大了
2022-07-26 -
服用抗生素后肠道菌群会发生什么变化?
2022-07-26 -
细菌沿着直线逃离狭小的空间
2022-07-26 -
新方法:在常规临床基因组测序分析中轻松识别肿瘤中的病毒
2022-07-26 -
颈动脉斑块内的个体免疫细胞特征
2022-07-26