经过多年的延迟FDA批准了Teva的通用EpiPen
一种蛋白质参与制造一种强效抗生素的图像揭示了抗生素合成的不寻常的第一步。宾州州立大学的化学家们领导的一项新的研究详细介绍了对这一过程背后化学成分的进一步了解,这将使研究人员能够将这种化合物和类似的化合物用于人类医学。
宾夕法尼亚州立大学的生物化学家、霍华德休斯医学研究所的研究员Squire Booker说:“抗生素硫链球菌对革兰氏阳性病原体非常有效,甚至可以在培养基中针对某些乳腺癌细胞。虽然它已被用于兽医局部,但到目前为止,它对人类无效,因为它的吸收不良。我们研究了硫链菌素生物合成的第一步,希望最终能够劫持某些过程,制造出可能具有更好药用性能的分子类似物。重要的是,这种反应在许多其他抗生素的生物合成过程中被发现,因此这项工作有可能影响深远。”
硫链菌素合成的第一步是甲基化。甲基被添加到反应的底物色氨酸分子中。参与色氨酸甲基化这种过程的主要系统之一涉及一类名叫自由基SAM蛋白的酶。
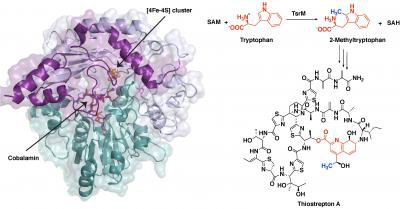
宾夕法尼亚州立大学化学系研究生、论文第一作者Hayley Knox说:“自由基SAM蛋白质通常利用一个铁硫簇来切割一个叫做S-腺苷-L-蛋氨酸(SAM)的分子,产生一个‘自由基’或一个有助于推进反应的未配对电子。到目前为止,我们所知道的一个例外是参与硫链菌素生物合成的蛋白质,称为TsrM。我们想知道为什么TsrM不做自由基化学,所以我们用X射线晶体学成像技术来研究它在整个反应过程中的几个阶段的结构。”
在迄今为止所描述的所有自由基SAM蛋白中,SAM直接与铁硫簇结合,这有助于使分子碎裂产生自由基。然而,研究人员发现SAM通常结合的部位在TsrM中被阻断。
Booker说:“这与任何其他激进的SAM蛋白完全不同。相反,结合到簇的SAM部分与色氨酸底物结合,并在反应中起关键作用,这就是所谓的底物辅助催化。”
研究人员在1月18日发表在《Nature Chemical Biology》杂志上的一篇文章中介绍了他们的研究结果。
在解决这个结构的过程中,研究人员能够推断出硫链菌素生物合成的第一部分,即色氨酸甲基化时的化学步骤。简言之,SAM的甲基转移到TsrM的钴胺素上。然后,在另一个SAM分子的帮助下,甲基转移到色氨酸,再生游离钴胺素并产生甲基化底物,这是合成抗生素的下一步所需。
“钴胺素是自然界中最强的亲核物质,这意味着它具有很强的反应性,”Knox说。“但是底物色氨酸是弱亲核的,所以一个大问题是钴胺素是如何被取代的。我们发现一个精氨酸残基位于钴胺素下面,使甲基钴胺素不稳定,从而使色氨酸取代钴胺素并甲基化。”
下一步,研究人员计划研究其他钴胺素依赖的自由基SAM蛋白,看看他们是否以类似的方式运作。最终,他们希望找到或创造出可以用于人类医学的硫链球菌素类似物。
Booker说:“TsrM在已知的钴胺素依赖的自由基SAM蛋白和自由基SAM蛋白方面显然是独特的。但是有成千上万的自由基SAM酶的独特序列,我们仍然不知道它们中的大多数是做什么的。随着我们继续研究这些蛋白质,我们可能会有更多的惊喜。”
原文检索:Structural basis for non-radical catalysis by TsrM, a radical SAM methylase
(生物通:伍松)
-
合成微生物使科学家们能够研究古老的进化神秘
2022-04-29 -
加强了恰帕斯高地土着居民的领土管理合作进程
2022-04-29 -
介绍CNVP,IUCN的新成员
2022-04-29 -
销售人员为肥胖客户推荐更多圆形产品
2022-04-29 -
黄石麋鹿的疾病隐藏成本 USU生态学家说 布鲁氏菌病会减少怀孕
2022-04-29 -
研究人员设计“智能”表面以排斥一切 但针对有益的例外
2022-04-29 -
大麻使用的性别差异开始在动物和人类的大脑研究的帮助下得到解释
2022-04-29 -
缅甸开始在全国红色名单上工作
2022-04-29 -
转染市场五年后将达到10亿美元
2015-07-08