经过多年的延迟FDA批准了Teva的通用EpiPen
3月22日,国际学术期刊Cell Reports在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)曾艺组和陈剑峰组的合作研究成果“procr functions as a signaling receptor and is essential for the maintenance and self-renewal of mammary stem cells”。该研究揭示了procr 作为受体向胞内传递信号通路从而调控乳腺干细胞的干性维持和自我更新的机制。
乳腺是由基底细胞和管腔细胞两层细胞构成的树状上皮导管组织,其发育主要发生在出生后。曾艺组此前的研究证明蛋白C受体procr标记的乳腺基底细胞是多潜能的乳腺干细胞,其在移植实验中具有极高的重构乳腺导管的能力,在体内谱系示踪实验中能够分化成基底细胞和管腔细胞(Wang et al., Nature 2015)。随后的实验发现 procr 在多种器官组织,包括血管内皮 (Yu et al., Cell Research 2016)、卵巢上皮 (Wang et al., Nature Communications 2019)、胰岛(Wang et al., Cell 2020)组织中标记成体干细胞。其它实验室的工作也证明procr在造血系统 (Balazs et al., Blood, 2006; Fares et al., Blood, 2017; Iwasaki et al., Blood, 2010; Zhou et al., Nature, 2016) 和皮肤 (Xue et al., Stem cells, 2017) 标记成体干细胞。然而,procr 是否仅仅是细胞表面标记?在干细胞中是否具有功能?它的胞内片段特别短(仅7个氨基酸),是否能作为信号受体往胞内传递信号?这些问题仍需要解决。
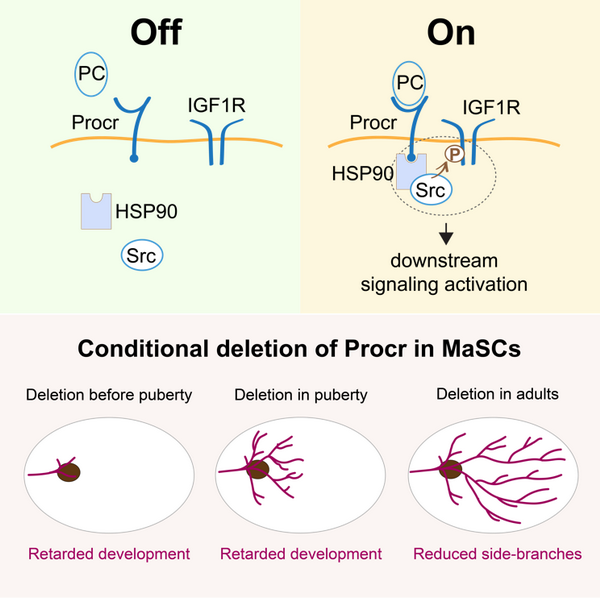
本研究构建了procr-flox 小鼠模型,发现在乳腺干细胞内条件性敲除 procr 导致乳腺的发育停滞,稳态维持被破坏,乳腺干细胞也丧失了在移植后重构器官的能力。在机制研究中,研究者利用质谱及co-Ip等实验发现,在配体蛋白C(pC)刺激后,procr 能够利用其胞内段与Hsp90aa1结合,并招募Src和IGF1R在膜上形成蛋白复合体,进一步激活IGF1R下游的Akt和ERK信号通路。体内、体外实验进一步验证了procr-Hsp90-Src-IGF1R通路在乳腺干细胞的特异激活性及重要性。在乳腺干细胞的体外培养体系中添加配体蛋白C能够促进乳腺克隆的形成和连续传代,而敲除Hsp90、用抑制剂抑制Src活性以及敲除IGF1R后,克隆形成能力明显降低。最后,利用procr-CreERT;Igf1r-flox小鼠,研究者证明在乳腺干细胞内敲除 Igf1r 得到和 procr-cKO 一致的乳腺发育停滞和稳态维持被破坏的表型。综上所述,这项工作阐明了 procr 作为信号转导的受体分子调控乳腺干细胞的干性维持和自我更新的分子机制,为理解 procr 在其它组织成体干细胞中的功能和机制具有重要的提示。
该研究由分子细胞卓越中心曾艺研究组和陈剑峰研究组合作完成。分子细胞卓越中心博士刘春业、林昶东、王代松和王经强为共同第一作者,曾艺研究员、陈剑峰研究员和贾莹莹副研究员为共同通讯作者。特别感谢多伦多大学许志忠教授对本研究提供的大力帮助。该项研究得到了分子细胞卓越中心公共技术服务中心动物实验技术平台、细胞生物学平台和分子生物学平台的支持。该工作获得科技部项目、中国科学院先导项目、国家基金委的大力资助。
文章链接:https://doi.org/10.1016/j.celrep.2022.110548
-
合成微生物使科学家们能够研究古老的进化神秘
2022-04-29 -
加强了恰帕斯高地土着居民的领土管理合作进程
2022-04-29 -
介绍CNVP,IUCN的新成员
2022-04-29 -
销售人员为肥胖客户推荐更多圆形产品
2022-04-29 -
黄石麋鹿的疾病隐藏成本 USU生态学家说 布鲁氏菌病会减少怀孕
2022-04-29 -
研究人员设计“智能”表面以排斥一切 但针对有益的例外
2022-04-29 -
大麻使用的性别差异开始在动物和人类的大脑研究的帮助下得到解释
2022-04-29 -
缅甸开始在全国红色名单上工作
2022-04-29 -
转染市场五年后将达到10亿美元
2015-07-08















