肿瘤释放乳酸,迫使附近的细胞发挥支持作用
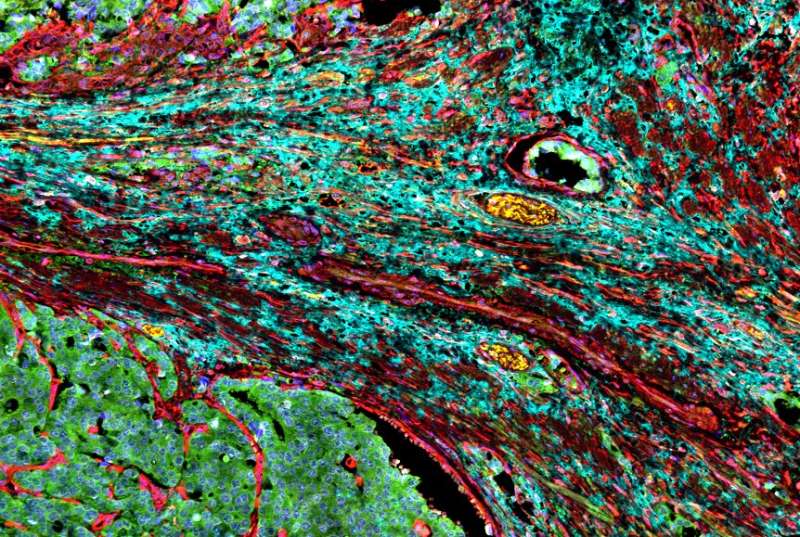
德克萨斯大学西南分校(UTSW)的研究人员报道,伤疤样细胞构成恶性胰腺肿瘤的很大一部分,保护这些癌症免受免疫攻击,它们来自组织和器官的间皮细胞。
他们的研究结果发表在《癌细胞》杂志上,题为“Mesothelial cell-derived antigen-presenting cancer-associated fibroblasts induce expansion of regulatory T cells in pancreatic cancer”。
研究人员写道:“最近的研究已经确定了一种独特的癌症相关的成纤维细胞(CAF)群体,称为抗原提呈CAFs (apCAFs),其特征是主要组织相容性复合体II类分子的表达,表明其在调节肿瘤免疫方面的功能。”“在这里,通过整合多个单细胞rna测序研究和进行强大的谱系追踪分析,我们发现apCAFs来自间皮细胞。”
他们的发现可能提供一种对抗胰腺癌的新策略。“通过靶向抗原提呈癌症相关的成纤维细胞,我们可能有一天能够显著增强胰腺癌患者免疫治疗的活性,”霍丛黄医学博士说,他是UTSW的外科讲师。黄博士与Rolf a . Brekken博士共同领导了这项研究,Rolf a . Brekken博士是外科、药理学教授,是犹他大学哈蒙肿瘤治疗研究中心的首席研究员,也是Harold C. Simmons综合癌症中心的成员。
研究人员早就知道,被称为CAFs的细胞构成了胰腺肿瘤的重要部分。黄解释说,尽管科学家们认为这些胰腺CAFs是一个统一的群体,但他和他在Brekken实验室的同事在2019年的一项研究中表明,这些细胞可分为三类。其中一种亚型被称为apCAFs,它通过在免疫细胞表面显示抗原蛋白与免疫细胞相互作用。
为了确定apCAFs如何促进pDA的进展,Huang、Brekken和他们的同事使用了一种被称为谱系追踪的技术来了解这些细胞是如何在正常胰腺发展为癌症时产生的。他们的发现表明,apCAFs来源于间皮细胞,间皮细胞形成一种保护膜,覆盖器官、体腔和组织。
进一步的实验表明,apCAFs表面的抗原可以将T细胞转化为一个称为调节性T细胞(regulatory T cells, Tregs)的亚群。当研究人员给携带胰腺肿瘤的小鼠注射针对间皮素(一种间皮细胞特有的蛋白质)的抗体时,treg的转化被阻断,使肿瘤更容易受到抗肿瘤免疫反应的攻击。
需要进一步的研究。然而,类似的策略可能有一天会被用于治疗人类的pDA,通过联合使用抗间皮素抗体和刺激免疫系统对抗癌症的免疫疗法。
原文标题:
Mesothelial cell-derived antigen-presenting cancer-associated fibroblasts induce expansion of regulatory T cells in pancreatic cancer
-
颈动脉斑块内的个体免疫细胞特征
2022-07-26 -
免疫系统癌症研究综述
2022-07-26 -
Nature子刊:根据大量神经成像数据预测大脑年龄
2022-07-26 -
将时间从几个月缩短到几周:一种新的基因传递方法
2022-07-26 -
《Science》四篇论文:绘制人类33个器官中的百万细胞
2022-07-26 -
Nature子刊:线粒体呼吸链维持炎症
2022-07-26 -
Nature子刊:基于电子病历预测心理健康危机的机器学习模型
2022-07-26 -
解决30年难题:科学家发现新的蛋白质结构,帮助合理设计药物
2022-07-26 -
Cell:发现首个在客户金属蛋白上装载锌的伴侣家族
2022-07-26 -
新的研究发现了与胶质母细胞瘤细胞发育有关的基因
2022-07-26