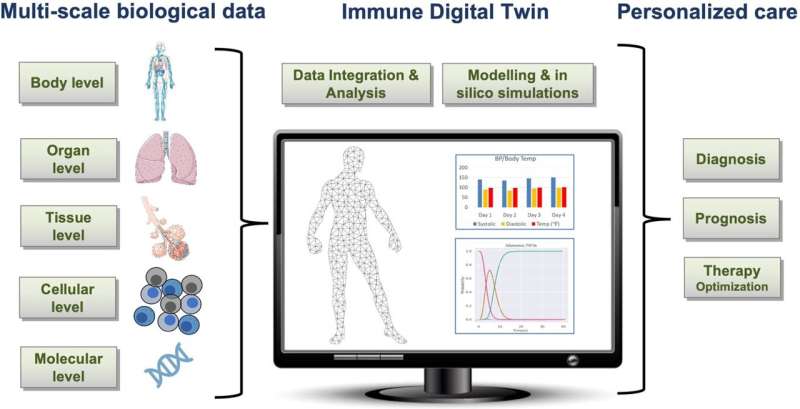
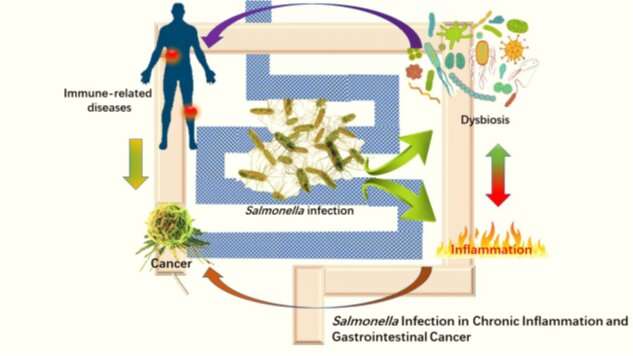
肿瘤释放乳酸,迫使附近的细胞发挥支持作用
细胞分裂的基因限制可能是老年人感染COVID-19后死亡的原因。与任何感染一样,人体免疫系统抗击COVID-19的能力在很大程度上取决于其复制免疫细胞的能力,这些细胞能够有效地摧毁导致疾病的SARS-CoV-2病毒。
虽然这些克隆的免疫细胞不能无限期地产生,但华盛顿大学(UW)的一项新研究提出了一个关键的假设,即人体产生这些克隆细胞的能力随着年龄的增长显著下降。
根据华盛顿大学研究教授詹姆斯·安德森(James Anderson)创建的一种新模型,这种对身体免疫系统的基因预先确定的限制可能是COVID-19对老年人造成毁灭性影响的关键。安德森是3月31日发表在《柳叶刀电子生物医学》杂志上的一篇论文的主要作者,该论文详细阐述了老龄化、COVID-19和死亡率之间的模型联系。
安德森指出,当DNA在细胞分裂中分裂时,端粒随着每次分裂而变短,“在一个细胞经过一系列复制后,它变得太短而停止进一步分裂。”不是所有细胞或所有动物都有这种局限性,但人类免疫细胞有这种细胞寿命。”据报道,Anderson是水产与渔业科学学院(水产与渔业科学学院)的一名生物系统建模师。
尽管有这个限制,一般人的免疫系统在大约50岁之前都能保持良好。当足够多的核心免疫细胞或T细胞有缩短的端粒时,它们不能通过细胞分裂足够快地克隆自己来攻击和清除COVID-19病毒——COVID-19病毒有一个显著的特征,可以减少免疫细胞的数量。
此外,安德森补充说,重要的是,端粒长度是遗传自父母的。所以每个年龄段的人在这些长度上都有一些差异。
安德森指出,在他的研究中,最重要的区别在于,对衰老的理解——即免疫系统用完整体端粒长度时,存在一个阈值——和所有人都会随着时间而变老的观点。令人兴奋的发现。
为了建立模型,研究人员使用了美国疾病控制中心和美国人口普查局公开的COVID-19死亡率数据,以及端粒研究。
结合一个人或一个特定群体的端粒长度信息,可以帮助医生知道谁更不容易受影响,安德森说。然后,它们可以根据哪些群体和个人可能更容易受到COVID-19的影响,分配资源,如援助剂。
安德森说:“我是一个建模师,我通过数学方程看到问题,我与生物学家一起工作来解释问题,但生物学家需要通过模型看到信息来指导他们的研究问题。”建模者的梦想是能影响伟大的生物学家像建模者一样思考。但这是困难。”
此外,Anderson还对模型提出了警告:“模型的每个参数都有大量的数据支持,而且对于如何从数据建立模型,有一个很好的逻辑思路。但它是如此简单,如此直观地吸引人。,以至于我们也应该对此持怀疑态度。作为一名科学家,我希望我们开始更多地了解作为自然选择一部分的免疫系统和群体反应。”
(来源:互联网,仅参考)
-
新方法:在常规临床基因组测序分析中轻松识别肿瘤中的病毒
2022-07-26 -
颈动脉斑块内的个体免疫细胞特征
2022-07-26 -
免疫系统癌症研究综述
2022-07-26 -
Nature子刊:根据大量神经成像数据预测大脑年龄
2022-07-26 -
将时间从几个月缩短到几周:一种新的基因传递方法
2022-07-26 -
《Science》四篇论文:绘制人类33个器官中的百万细胞
2022-07-26 -
Nature子刊:线粒体呼吸链维持炎症
2022-07-26 -
Nature子刊:基于电子病历预测心理健康危机的机器学习模型
2022-07-26 -
解决30年难题:科学家发现新的蛋白质结构,帮助合理设计药物
2022-07-26 -
Cell:发现首个在客户金属蛋白上装载锌的伴侣家族
2022-07-26