经过多年的延迟FDA批准了Teva的通用EpiPen
NG2胶质细胞,又名少突胶质前体细胞(Oligodendrocyte precursor cells,OpCs),具有分化生成成熟少突胶质细胞的能力,在大脑早期发育的髓鞘形成过程中起重要作用。然而在髓鞘化基本完成的成年大脑中,NG2胶质细胞仍占神经细胞总数的4% - 9%,提示其在中枢神经系统中还有着其他未被发现的重要功能。与大脑中其它胶质细胞不同,NG2胶质细胞是目前唯一一类被报道能与神经元建立直接突触联系并接收神经元突触传入的神经胶质细胞。然而关于NG2胶质细胞与神经元之间的突触连接是否具有双向性,以及其在神经网络中的功能研究还知之甚少。
2021年9月30日,上海交通大学医学院童小萍研究团队在Nature Communications杂志上在线发表了题为NG2 glia-derived GABA release tunes inhibitory synapses and contributes to stress-induced anxiety的最新研究成果。在此项工作中,作者率先揭示了NG2胶质细胞突触调控的新机制。

该项研究发现,小鼠海马区NG2胶质细胞可以特异性调控邻近中间神经元的抑制性突触传入,并且应用双标记法免疫电镜技术首次报道了NG2胶质细胞作为突触前与神经元形成的抑制性突触样结构。结合光电联合记录、转录组测序、RNA scope原位杂交,以及全内反射荧光显微镜成像等技术,进一步证实了NG2胶质细胞可以通过VAMp2囊泡转运方式介导抑制性神经递质γ-氨基丁酸(GABA)释放,并且含有GABA合成的关键酶——谷氨酸脱羧酶GAD67。提示NG2胶质细胞具有合成GABA的能力,在被激活的情况下可以通过突触囊泡释放GABA调控中间神经元的突触活动。
在生理病理功能方面,该研究发现海马区NG2胶质细胞在焦虑小鼠中的活动频率明显提高,表现为钙活动明显增强。当主动激活海马区NG2胶质细胞时,可以通过增强对中间神经元的抑制性突触调控机制最终引起局部神经微环路的兴奋-抑制性失衡,诱发小鼠产生焦虑样行为,提示了NG2胶质细胞与焦虑相关疾病的发生和发展有着密切联系。
该项研究从分子、细胞、神经微环路及在体行为学分析等多维度揭示了NG2胶质细胞与神经元间交互作用的神经机制以及对维持神经网络正常功能的重要性,为临床上治疗焦虑相关疾病提供了新的思路和理论依据。
上海交通大学基础医学院童小萍研究员为本文的通讯作者,博士生张潇、刘瑶和助理研究员洪小琦为本文的共同第一作者。该研究得到了国家基金委、科技部、上海市教委、上海市科委等课题的资助。
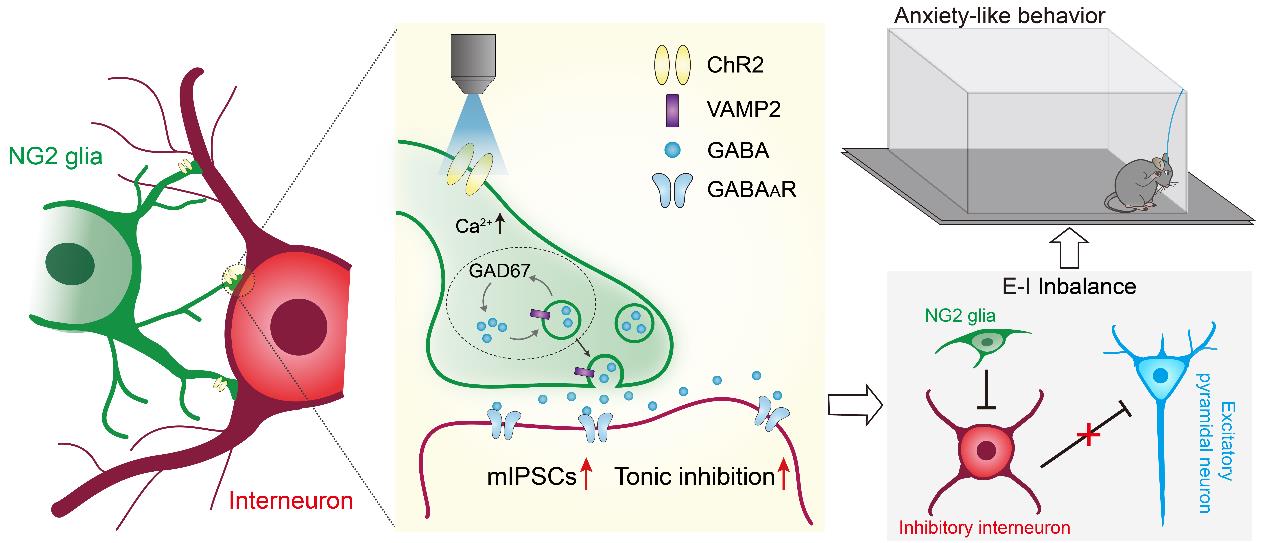
图1 NG2胶质细胞在海马区参与抑制性突触调控的机制图
-
合成微生物使科学家们能够研究古老的进化神秘
2022-04-29 -
加强了恰帕斯高地土着居民的领土管理合作进程
2022-04-29 -
介绍CNVP,IUCN的新成员
2022-04-29 -
销售人员为肥胖客户推荐更多圆形产品
2022-04-29 -
黄石麋鹿的疾病隐藏成本 USU生态学家说 布鲁氏菌病会减少怀孕
2022-04-29 -
研究人员设计“智能”表面以排斥一切 但针对有益的例外
2022-04-29 -
大麻使用的性别差异开始在动物和人类的大脑研究的帮助下得到解释
2022-04-29 -
缅甸开始在全国红色名单上工作
2022-04-29 -
转染市场五年后将达到10亿美元
2015-07-08















