经过多年的延迟FDA批准了Teva的通用EpiPen
近日,厦门大学药学院Dieter A. Wolf教授课题组在Cell子刊Cell Chemical Biology在线发表题为“Metabolic targeting of cancer by a ubiquinone uncompetitive inhibitor of mitochondrial complex I”的研究论文。研究发现小分子化合物SMIp004-7及其细胞色素p450酶依赖性活化代谢物具有非竞争性的抑制机制,涉及催化亚基NDUFS2的独特N端区域,导致线粒体复合物I的快速分解。该小分子化合物可有效靶向干细胞样的耐药细胞,抑制三阴性乳腺癌移植瘤增殖,逆转肿瘤缺氧,并促进肿瘤免疫监测。
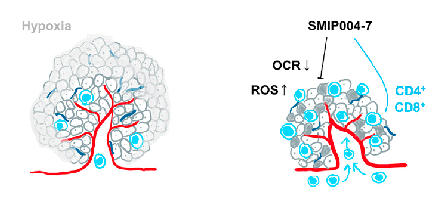
能量代谢异常是癌细胞最基本的特征之一。虽然最初的研究集中在糖酵解方面,但线粒体氧化磷酸化(OXpHOS)已成为耐药癌细胞的主要靶点,因此靶向癌细胞代谢脆弱性正成为抗肿瘤新药开发的新方向,OXpHOS抑制剂有望成为治疗癌症的新型药物。
Wolf教授课题组最早于2013年发现小分子化合物SMIp004-7可作为有效的线粒体呼吸抑制剂,前期的研究发现SMIp004-7特异性抑制线粒体复合物I,且葡萄糖限制可增强此小分子对癌细胞的细胞毒性,而促进线粒体复合物I活性以及过表达NDUFS2则可挽救其细胞毒性。酶动力学实验表明SMIp004-7不同于其他线粒体复合物I的抑制剂,它是以非竞争性的方式靶向线粒体复合物I,并且其细胞色素p450酶的代谢产物具备更强的生物活性。小鼠三阴性乳腺癌荷瘤实验表明,SMIp004-7的抗肿瘤活性是由宿主免疫功能促进的。SMIp004-7可抑制肿瘤的线粒体复合物I活性,从而通过抑制肿瘤细胞线粒体呼吸来逆转肿瘤缺氧,改善肿瘤微环境,并促进肿瘤内部CD4+, CD8+ T细胞的浸润。同时,SMIp004-7与抗pD-1联用显著增强抗肿瘤活性。SMIp004-7在线粒体中分子靶标的鉴定,为进一步推动该化合物作为潜在癌症治疗药物的研究奠定了基础,并且为OXpHOS抑制剂的研究提供了一个新的思路。
厦门大学药学院博士生胡程为该论文的共同第一作者, Dieter A. Wolf教授和程亚彬助理教授为共同通讯作者,博士毕业生田贵游和硕士毕业生柯蔚参与了该项目研究。该研究工作获得了国家自然科学基金面上项目(81773771),福建省科技厅基金(2018J01053)等经费的支持。
论文链接:
https://www.sciencedirect.com/science/article/pii/S2451945621004797
https://pubmed.ncbi.nlm.nih.gov/34852219/
(图/文:厦大药学院)
-
合成微生物使科学家们能够研究古老的进化神秘
2022-04-29 -
加强了恰帕斯高地土着居民的领土管理合作进程
2022-04-29 -
介绍CNVP,IUCN的新成员
2022-04-29 -
销售人员为肥胖客户推荐更多圆形产品
2022-04-29 -
黄石麋鹿的疾病隐藏成本 USU生态学家说 布鲁氏菌病会减少怀孕
2022-04-29 -
研究人员设计“智能”表面以排斥一切 但针对有益的例外
2022-04-29 -
大麻使用的性别差异开始在动物和人类的大脑研究的帮助下得到解释
2022-04-29 -
缅甸开始在全国红色名单上工作
2022-04-29 -
转染市场五年后将达到10亿美元
2015-07-08















